Differenzierung und Proliferation von Zellen während der Entwicklung und Regeneration
Forschungsbericht (importiert) 2004 - Max-Planck-Institut für Herz- und Lungenforschung - W. G. Kerckhoff-Institut
1. Differenzierung und Proliferation von Zellen während der Entwicklung und Regeneration
Molekulare Kontrolle der Differenzierung und Regeneration im geschädigten und alternden Herzen
Nach allgemeiner Lehrmeinung besteht das adulte Herz aus ausdifferenzierten Kardiomyozyten (Herzmuskelzellen), die nicht mehr teilungsfähig sind. Da das menschliche Herz über Dekaden hinweg kontinuierlich und effizient arbeiten kann, wurde angenommen, dass individuelle Kardiomyozyten diesen Zeitraum ebenfalls ohne große Veränderungen überleben. Verschiedene Arbeiten zeigten jedoch, dass das Altern und Schädigungen des Herzens unausweichlich zum Verlust von Zellen durch den sog. programmierten Zelltod (Apoptose) mit folgenden Gewebeveränderungen (Nekrosen) führen. Hieraus kann geschlossen werden, dass adulte Kardiomyozyten noch eine Restfähigkeit zur Selbst-Erneuerung haben und dass diese für die Aufrechterhaltung einer normalen Herzfunktion essentiell ist. Bislang ist nicht bekannt, welche Signale und Prozesse die Balance von Zelltod, Zellüberleben und Zellteilung bestimmen.
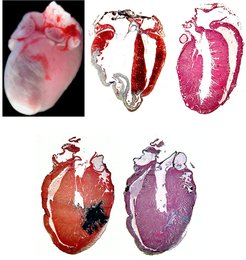
Eine Arbeitsgruppe am MPI für Herz- und Lungenforschung in Bad Nauheim sucht nach Wachstumsfaktoren, die dieses empfindliche Gleichgewicht kontrollieren könnten. Einer dieser Faktoren ist möglicherweise BMP-10, ein neues Mitglied der BMP-Familie (bone morphogenetic proteins), das spezifisch in den "Trabekel" genannten Muskelbällchen im Herzgewebe und dem Atrium (Herzvorhof) des sich entwickelnden Mausherzens exprimiert wird. Homozygot-mutante BMP-10-Mäuse entwickeln eine frühe Dysfunktion des Herzens, was insbesondere durch eine fehlende Trabekulierung bedingt sein könnte, die zu einem Absterben der mutanten Embryonen zwischen E10.5 und 11.5 p.c. (nach Begattung) führt. In der Gewebekultur schützen BMPs zudem die Kardiomyozyten vor Apoptose. Da BMP-10 in adulten Maus- und Menschenherzen hochgradig exprimiert ist, werden die Forscher die Rolle von BMP-10 beim Überleben und Altern der Kardiomyozyten in transgenen Mausmodellen analysieren. Sie erwarten, dass ein tieferes Verständnis der Rolle von BMPs zu neuen therapeutischen Methoden bei Herzkrankheiten führt (Abb.1).
Reparaturprozesse im alternden oder geschädigten Herzen sind durch die Generierung von nicht-funktionalem Narbengewebe charakterisiert. Eine Regeneration von alternden Herzen ist – wie oben ausgeführt – durch die Einschränkung der Teilungsfähigkeit von adulten Herzmuskelzellen und das Fehlen von ausreichender Mengen an Herzstammzellen nicht möglich. Die Wissenschaftler am MPI versuchen daher, den mitotischen Block der Kardiomyozyten durch Manipulation der Zell-Maschinerie aufzuheben. Hierbei untersuchen sie besonders die Rolle der Transkriptionsfaktoren E2F und der katalytischen Untereinheit des Enzyms Telomerase für die Initiierung des Zellzyklus sowie den potenziellen Einsatz von dominant negativen Versionen von p53 und p73 für die Verhinderung der Apoptose von Herzmuskelzellen.
Forscher: Izabella Pietrowska, Thomas Kubin, Zhipei Liu
Herzregeneration des Grünen Wassermolches (Notophtalmus viridescens)

Einige Organismen haben die Fähigkeit, Zellen, die in anderen Spezies postmitotisch sind, zum Wiedereintritt in den Zellzyklus zu bewegen und sogar ganze Organe bzw. Organteile neu zu bilden. Ein bekanntes Mitglied dieser Tierfamilie ist der Molch Notophtalmus viridescens, der für seine Fähigkeit bekannt ist, amputierte Gliedmaßen oder Schwänze und einige andere Strukturen zu regenerieren. N. viridescens ist einer der wenigen Vertebraten, der auch in der Lage ist, Herzmuskelgewebe zu regenerieren (Abb. 2). Ein Wissenschaftler-Team am MPI in Bad Nauheim vergleicht Expressionsprofile von ungeschädigtem und regenerierendem Herzgewebe, um Moleküle zu identifizieren, die die Regenerationsfähigkeit des Molchherzens steuern. Daten aus diesem Screening werden mit Resultaten ähnlicher Screens eines Mausmodells für Herzinfarkt verglichen. Bislang haben die Forscher DNA-Chips mit 100 000 cDNAs generiert und zur Identifizierung von Genen eingesetzt, die eine differentielle Expression im regenerierenden und ruhenden Herzen zeigen. Eine detaillierte funktionelle Analyse des molekularen Pfades, der die Herzregeneration in Molchen bestimmt, ist der nächste Schritt, der zurzeit über verschiedene Herangehensweisen realisiert wird.
Forscher: Thilo Borchadt, Julia Kruse, Thomas Kubin, Thomas Böttger, Rene Zimmermann
Identifizierung von Genen, die die Differenzierung von Kardiomyozyten kontrollieren
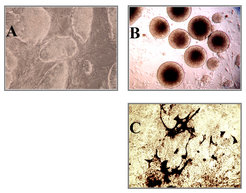
In der Vergangenheit wurden bereits verschiedene Gene identifiziert, die zur Differenzierung von Kardiomyozyten und zur Morphogenese des Herzens beitragen. Dennoch ist es sehr wahrscheinlich, dass eine deutlich größere Anzahl von Genen für die spezifische Gestaltwerdung des Herzens eine Rolle spielt. Umfassende funktionelle Ansätze, derartige Gene zu identifizieren, existieren für Säuger bislang nicht. Eine Forschergruppe am MPI wendet eine Genome-Wide-Screen-Strategie an, die auf der Differenzierung embryonaler Stammzellen basiert. Sie nutzt komplexe retrovirale siRNA-Bibliotheken, um Gene zu identifizieren, die eine ausschlaggebende Rolle bei der Differenzierung von Kardiomyozyten spielen. Die identifizierten Gene werden bei der Differenzierung von embryonalen Stammzellen (ES-Zellen) in vitro mittels Formation von Embryoid Bodies (EBs; Abb. 3B) und in vivo unter Nutzung von tetraploid aggregierten Chimären untersucht.
Forscher: Andre Schneider, Thomas Böttger, Dietmar von der Ahe
Herzalterung und oxidativer Stress: SIR-Gene und die Kontrolle des Energiemetabolismus
Reaktive Sauerstoffspezies (ROS=Sauerstoffradikale) bewirken eine Vielzahl degenerativer Veränderungen in der Zelle und führen zu vorzeitiger Zellalterung. Im Allgemeinen wird die Anhäufung von ROS als Hauptgrund für verstärkte Zellalterung angesehen. Gewebe, die hauptsächlich aus postmitotischen Zellen bestehen, scheinen für die Schädigung durch ROS besonders anfällig zu sein, da sie nur ein limitiertes Regenerationspotenzial besitzen. Bislang sind die exakten Zusammenhänge zwischen oxidativem Stress und Alterung nicht vollständig bekannt Abb. 4. Es ist jedoch klar, dass erhöhter oxidativer Stress zu einer Instabilität des Energiemetabolismus führt. Der unbalancierte Energiemetabolismus zieht wahrscheinlich eine reduzierte Aktivität der SIR- (silent information regulator) Genfamilie nach sich. Die SIR-Gene inaktivieren vermutlich spezielle Chromatindomänen (durch die Deacetylierung NAD-abhängiger Histone) und üben dadurch eine Schutzfunktion aus. Dieser Vorstellung entsprechend führt die Über-Expression von SIR2 in der Hefe (Saccharomyces cervisiae) zu einem deutlichen Anstieg der Lebensdauer.
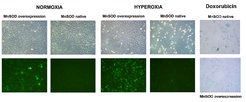
Wissenschaftler am MPI für Herz- und Lungenforschung haben verschiedene Mauslinien generiert, die es ihnen ermöglichen, die Rolle des oxidativen Stresses, des Alterns und der Chromatin-Inaktivierung zu untersuchen. Hierfür konstruierten sie ein konditionell aktives Allel von SOD2 (Superoxiddismutase), das die Inaktivierung und Aktivierung des Gens zu bestimmten Zeitpunkten im Herzmuskel ermöglicht. In einer zweiten Versuchsreihe wird SIR2-cDNA im Herzen künstlich überexprimiert. Weiterhin erforschen sie den Effekt von normalkalorischer und hypokalorischer Nahrung auf oxidativen Stress und die Zellalterung unter Nutzung entsprechender Expressionsprofile von Kardiomyozyten. Sie analysieren zudem die Verbindung zwischen oxidativem Stress und Genchromatin-Inaktivierung durch die Kreuzung SOD2-defizienter Mäuse mit solchen, in denen SIR2 überexprimiert ist.
Forscher: Eva Bober, Susanne Weinlich, Olesya Vakrusheva
Kontrolle der Migration von Muskelvorläuferzellen durch induktive und autonome Signale der Zelle
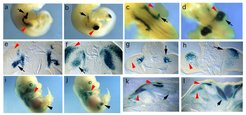
Die Migration ist eine wichtige Eigenschaft der myogenen Zellen (Muskelvorläuferzellen) während der Organogenese und Organregeneration. In der Vergangenheit konnten die Forscher zeigen, dass das Homeobox-Gen Lbx1 die Migration von Muskelvorläuferzellen in den Gliedmaßen auf zell-autonome Weise reguliert. Ihre Ergebnisse bewiesen, dass Lbx1 ein Schlüsselregulator der Muskelvorläuferzellmigration ist und für die gezielte Migration von Vorläuferzellen der hinteren Gliedmaßenmuskeln und der Streckermuskeln der Vordergliedmaßen benötigt wird (Abb. 5). Mittels cDNA-Subtraktion hetero- und homozygot mutanter Lbx1-Zellen konnten die Wissenschaftler verschiedene putative Zielgene von Lbx1 identifizieren. Die funktionelle Untersuchung dieser Gene ist zurzeit in Arbeit. Weiterhin untersucht die Arbeitsgruppe Signaltransduktionskaskaden, die für die Zellbeweglichkeit und Migration von Muskelvorläuferzellen in adulten Mäusen und Hühnerembryonen nötig sind.
Forscher: Stefan Günther, Svetlana Oustanina
Regulation des Körpergewichts und der Herzfunktion durch neuronale bHLH-Gene
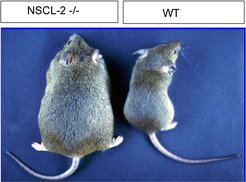
Im Rahmen eines Screenings nach neuronal exprimierten bHLH-Genen (Transkriptionsfaktoren, die eine basische Helix-Loop-Helix-Domäne enthalten) konnten Forscher des MPI in Bad Nauheim vor einigen Jahren eine Reihe verschiedener cDNAs und Gene identifizieren. Insbesondere analysieren sie die beiden Gene NSCL1 und NSCL2. Obgleich die Inaktivierung von NSCL1 keine auffallenden neuronalen Dysfunktionen zur Folge hatte, sterben NSCL1-mutante Mäuse vorzeitig, vermutlich in Folge kardialer Dysfunktionen, die eventuell durch vegetative Fehlfunktionen ausgelöst werden. NSCL2-defiziente Mäuse leiden zudem unter multiplen neuroendokrinen Störungen (Abb. 6). Die kombinierte Inaktivierung beider Gene führt zu einer verringerten Nervenzellproliferation und gestörter Differenzierung im olfaktorischen Epithel.
Die Forscher interessieren sich für die molekularen und physiologischen Prozesse, die diesen Phänotypen zugrundeliegen. Besonderes Augenmerk wird auf die Analyse von NSCL1- und NSCL2-Target-Genen und auf die Verbindung von Zellproliferation und -differenzierung gelegt. Ein Schwerpunkt der künftigen Aktivitäten in diesem Projekt liegt in der Untersuchung der Funktion von NSCL2 im adulten Organismus und dem Mechanismus der Herzrhythmusabnormalitäten und vegetativen Dysfunktionen in NSCL1-Mutanten.
Forscher: Karen Ruschke, Thomas Schmidt
2. Verbesserung und Beschleunigung der Geweberegeneration: Reparatur und Ersatz von geschädigten Herz- und Skelettmuskelzellen
Regenerative Medizin ist ein neues und reizvolles Feld der biologischen und medizinischen Forschung. Sie basiert direkt auf Resultaten der Grundlagenforschung, die Zelldifferenzierung und -entwicklung betreffen. Neuere Erkenntnisse gehen davon aus, dass vorangegangene Entscheidungen von Zellen nicht unumkehrbar sind, sondern rückgängig gemacht und geändert werden können. Ein solches „dynamisches Konzept der Identitätsfindung“ einer Zelle basiert auf der Idee, dass die Erhaltung eines zellulären Phänotyps kontinuierlicher Regulation bedarf. Im Prinzip bedeutet dies, dass es möglich sein sollte, ausdifferenzierte Zellen zu re-programmieren und so die regenerativen Eigenschaften von Gewebe und Organen zu verstärken.
Selektion und Manipulation von mesenchymalen Stammzellen zur Generierung von Myoblasten und Kardiomyozyten
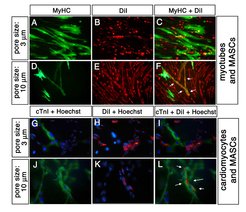
Mesenchymale Stammzellen (MSCs) treten im Stroma (Stützgewebe) verschiedener Organe auf. Das Knochenmark enthält MSCs, die in der Lage sind, Eigenschaften verschiedener Zelltypen, inklusive Herz- und Skelettmuskeln sowie neuroektodermaler Zellen, anzunehmen (Abb. 7). Der Gebrauch von genetisch markierten, aus Knochenmark abgeleiteten MSCs ermöglichte es den Forschern, einen Einblick in das Differenzierungspotenzial von MSCs in vivo nach Injektion in frühe Mausembryonen zu nehmen. Durch die Kombination von spezifischen genetischen Selektionsstrategien und Induktionsprotokollen ist es gelungen, relativ uniforme Zellpopulationen herzustellen, die Charakteristika von Muskelzellen aufweisen und gegebenenfalls für therapeutische Zwecke eingesetzt werden können.
Weiterhin arbeitet die Gruppe an der Optimierung der Methoden für eine effiziente Selektion und Expansion von MSCs zur Generierung von Myoblasten und Kardiomyozyten. Außerdem bestimmen sie das therapeutische Potenzial dieser Zellen. Ein solcher Ansatz kann jedoch nur dann erfolgreich sein, wenn es gelingt, mehr über die Signale und Prozesse zu lernen, die zur Determination und Differenzierung in verschiedene Zelllinien notwendig sind.
Forscher: Fikru Belema Bedada, Kerstin Broich
Satellitenzellen: Kontrolle der Proliferation, Zellzyklusaustritt und Differenzierung während der Geweberegeneration
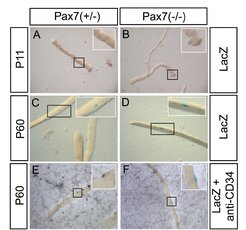
Satellitenzellen sind die Stammzellen der Skelettmuskeln. Sie sind zwischen der Basallamina und der Plasmamembran (Sarkolemma) von Myotuben lokalisiert, wo sie bei körperlicher Betätigung, Muskelverletzungen oder Erkrankungen, die zur Schädigung von Muskelfasern führen, aktiviert werden. Die Wissenschaftler analysieren die Mechanismen, die die Proliferation, den Zellzyklusaustritt und die Differenzierung von Satellitenzellen während der Muskelgeweberegeneration kontrollieren (Abb. 8). Mittels Transplantation genetisch markierter Zellen aus Mausmutanten mit gezielten Mutationen in der Familie der FGF-Wachstumsfaktorgene zeigten sie, dass myogene Stammzellen in autokriner Weise von FGFs abhängig sind. Die Nutzung von dominant negativen Retroviren lässt vermuten, dass FGFs eine ras- und ral-abhängige Kaskade in Gang setzen, die die Zellmigration einleitet.
Die Forscher bestimmen das Potenzial generischer und genetisch veränderter Wachstumsfaktoren für die Therapie und Prävention von Skelettmuskelkrankheiten in transgenen Tieren als prä-klinisches Modell. Zwei verschiedene Ansätze werden angewandt: 1) Generierung transgener Tiermodelle für die Analyse der Funktion der Wachstumsfaktoren, in erster Linie von FGFs, Myostatin und SF/HGF; 2) Selektion von genetisch veränderten Wachstumsfaktoren auf Myostatin-Basis mit einem veränderten biologischen Spektrum. Die Analyse der Wachstumsfaktoren während der Regeneration wird durch Experimente unterstützt, die die Funktion von zellautonomen Prozessen bei der Aktivierung und Erhaltung von Satellitenzellen zum Gegenstand haben.
Forscher: Svetlana Oustanina, Michal Mielcarek, Stefan Günther, André Schneider







